出口欧盟必备 口罩等防护产品除了CE认证,还需关注MDD/MDR合规
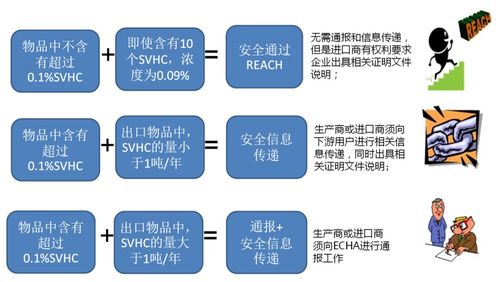
随着全球对防护产品的持续需求,中国制造企业正积极拓展欧盟市场。杭州昇迪科技等网络技术服务公司发现,许多出口商在口罩、防护服等产品出口欧盟时,往往只关注CE认证,却忽略了另一个至关重要的合规要求——医疗器械法规(MDR)或医疗器械指令(MDD)下的产品分类与认证。
口罩、护目镜、防护服等个人防护设备(PPE)在欧盟市场销售,确实需要获得CE认证,以证明其符合欧盟的安全、健康和环保要求。这类产品若在医疗环境下使用(如医用外科口罩、FFP2/FFP3防护口罩等),则被欧盟定义为医疗器械,必须同时满足医疗器械相关法规。
根据欧盟医疗器械法规(MDR 2017/745),医疗器械按风险等级分为I类、IIa类、IIb类和III类。其中,外科口罩通常属于I类医疗器械,而高风险防护口罩可能被归为IIa或IIb类。企业需根据产品分类,选择相应的合格评定程序:
- I类低风险产品可进行自我符合性声明。
- IIa类及以上产品则必须通过欧盟公告机构进行认证,包括技术文件审核和可能的现场审查。
杭州的网络技术服务公司提醒出口企业,忽视MDR/MDD要求可能导致产品被海关扣留、市场禁入甚至法律风险。为此,企业应:
- 明确产品用途和分类,确定适用CE认证(PPE指令)还是MDR/MDD。
- 准备完整的技术文件,包括产品设计、制造流程、风险评估、临床数据等。
- 选择有资质的公告机构进行认证,并确保生产符合质量管理体系(如ISO 13485)。
- 关注法规更新,MDR已逐步取代MDD,过渡期至2024年,企业需及时调整合规策略。
出口欧盟的防护产品合规是一个系统工程,CE认证只是入门券。企业需结合产品特性,全面满足MDR等法规要求,并借助专业服务机构(如杭州昇迪科技提供的技术咨询)确保顺利进入欧盟市场。
如若转载,请注明出处:http://www.jia027.com/product/52.html
更新时间:2026-05-23 12:12:53